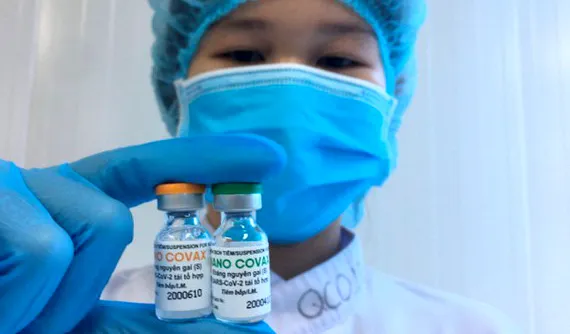
Ngày 22-6, đại diện Công ty Cổ phần Dược sinh học Nanogen (Công ty Nanogen) cho biết vừa có văn bản gửi Thủ tướng Chính phủ, xin cấp phép khẩn cấp vaccine NanoCovax.
Công ty Nanogen đã nghiên cứu và sản xuất vaccine NanoCovax phòng Covid-19 năm 2020 trong tình hình dịch Covid-19 diễn biến phức tạp. Vaccine đã chứng minh được những thành công bước đầu, dựa trên các kết quả báo cáo giữa kỳ của thử nghiệm lâm sàng giai đoạn 1 và 2, đã được Hội đồng đạo đức trong nghiên cứu y sinh chấp thuận và đánh giá tốt.
Đồng thời, Bộ Y tế và Hội đồng đã thông qua đề cương nghiên cứu, triển khai thử nghiệm lâm sàng giai đoạn 3 cho NanoCovax hàm lượng 25mecg/ml, trên quy mô 13.000 người.
Dựa trên các kết quả thử nghiệm lâm sàng, khả năng sinh miễn dịch của vaccine NanoCovax đạt 99,4%. So sánh với các loại vaccine khác trên thế giới là không hề thua kém và có phần cao hơn. Dù vậy, giá bán dự kiến hiện đang thấp nhất thế giới, chỉ với 120.000 đồng/liều.
 Ông Hồ Nhân, Tổng giám đốc Công ty Nanogen đang giới thiệu về cơ chế của vaccine NanoCovax. Ảnh: HOÀNG HÙNG
Ông Hồ Nhân, Tổng giám đốc Công ty Nanogen đang giới thiệu về cơ chế của vaccine NanoCovax. Ảnh: HOÀNG HÙNG
Công suất sản xuất hiện nay của nhà máy Nanogen đạt 8 triệu đến 12 triệu liều/tháng. Công ty cũng đang hoàn thiện, mở rộng hệ thống kho lạnh với sức chứa 10 triệu liều cũng như đội ngũ xe lạnh (từ 2 đến 8°C) vận hành đạt chuẩn quốc tế.
Dựa trên kế hoạch và năng lực hiện tại, công ty dự kiến cung cấp đủ 50 triệu liều đến tháng 12-2021 và 100 triệu liều vào năm 2022.
Nanogen khẳng định quyết tâm đẩy mạnh nghiên cứu, sản xuất cung cấp đủ vaccine để Việt Nam đạt được miễn dịch cộng đồng vào quý II-2022. Công ty có kiến nghị Chính phủ để vaccine NanoCovax sớm được cấp phép khẩn cấp có điều kiện, tương tự như các loại vaccine của Nga, Trung Quốc và Ấn Độ.
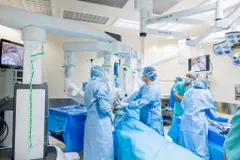
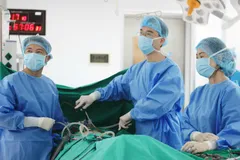
 Nhân viên Công ty Nanogen đang tích cực nghiên cứu, sản xuất vaccine NanoCovax. Ảnh: HOÀNG HÙNG
Nhân viên Công ty Nanogen đang tích cực nghiên cứu, sản xuất vaccine NanoCovax. Ảnh: HOÀNG HÙNG
Trước đó, ngày 11-6, Bộ Y tế đã có Quyết định số 2899/QĐ-BYT về việc phê duyệt đề cương nghiên cứu thử nghiệm lâm sàng giai đoạn 3 vaccine NanoCovax phòng Covid-19. Tổ chức nhận thử nghiệm lâm sàng là Học viện Quân Y và Viện Pasteur TPHCM; địa điểm triển khai tại Học viện Quân Y, tỉnh Hưng Yên, Viện Pasteur TPHCM, tỉnh Long An, tỉnh Tiền Giang và một số đơn vị đủ điều kiện theo quy định tại các tỉnh triển khai nghiên cứu.
Đối tượng nghiên cứu từ 18 tuổi trở lên đáp ứng đầy đủ các tiêu chuẩn lựa chọn, và không có bất kỳ tiêu chuẩn loại trừ nào theo đề cương nghiên cứu. Số lượng đối tượng tham gia nghiên cứu thử nghiệm lâm sàng giai đoạn 3 dự kiến khoảng 13.000 người, để đánh giá tính an toàn, đáp ứng miễn dịch và hiệu lực bảo vệ của vaccine (bao gồm 1.000 đối tượng để đánh giá giữa kỳ về tính an toàn và sinh miễn dịch).
TS-BS Phạm Quang Thái, Trưởng Văn phòng tiêm chủng miền Bắc, Phó trưởng Khoa Kiểm soát bệnh truyền nhiễm, Viện Vệ sinh dịch tễ Trung ương, cho biết vaccine NanoCovax đã chứng minh được trên thử nghiệm lâm sàng, tạo ra kháng thể mạnh, trung hòa được cả những chủng mới.
Như vậy, Việt Nam đã tiệm cận với khả năng chúng ta tự có sản phẩm vaccine của riêng mình để chống lại Covid-19. Tuy nhiên, để có thể sản xuất một khối lượng lớn trong thời gian sớm, chúng ta cần có sự hỗ trợ từ Chính phủ và các nhà tài trợ...
| Qua các lần thử nghiệm, cả 3 liều vaccine Nanocovax 25mcg, 50mcg, 75mcg đều an toàn, biến cố bất lợi đa số nhẹ (độ 1), hết nhanh sau khoảng 2-3 ngày sau tiêm. Đặc biệt, so sánh giữa các biến cố bất lợi của các vaccine đã được cấp phép trên thế giới, nhà sản xuất ghi nhận NanoCovax có tỷ lệ phản ứng tại chỗ và toàn thân sau khi tiêm tương tự. Tính hiệu quả rất khả quan khi dự kiến đạt trên 80%, trong khi giá khoảng 120.000 đồng/liều. |