Theo đó, hội đồng gồm hơn 10 thành viên, gồm các chuyên gia về dịch tễ, lâm sàng, vắc xin, thuốc..., đứng đầu là PGS-TS Lê Văn Truyền - nguyên thứ trưởng Bộ Y tế, chuyên gia cao cấp về dược - sẽ dành cả ngày 29-8 họp xem xét hồ sơ 2 vaccine, gồm 1 vaccine nhập khẩu và 1 vaccine trong nước. Trong đó, vaccine trong nước là Nano Covax.
Thông tin ban đầu từ trước phiên họp, cho biết Hội đồng Đạo đức trong nghiên cứu y sinh quốc gia đã thông qua báo cáo thử nghiệm lâm sàng giữa kỳ giai đoạn 3a, điều kiện cần theo hướng dẫn mới, để có thể xem xét hồ sơ Nano Covax.
Cũng có ý kiến cho biết hồ sơ trình hội đồng xem xét trên báo cáo dữ liệu trước và sau tiêm 1.000 người tham gia thử nghiệm giai đoạn 3a, là con số "thấp hơn" so với các vắc xin đã được phê duyệt khẩn cấp sau thử nghiệm giai đoạn 3 trên thế giới.
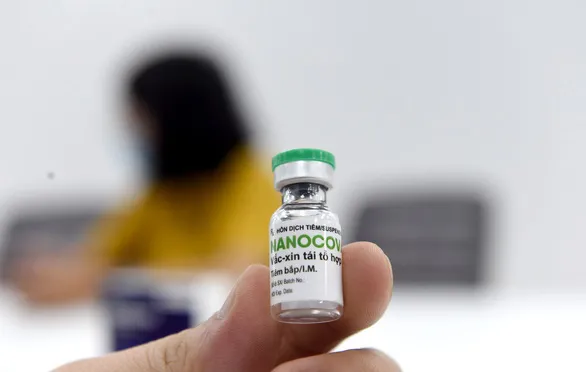 Vaccine Nano Covax của Nanogen. Ảnh: Duyên Phan
Vaccine Nano Covax của Nanogen. Ảnh: Duyên Phan Cho đến nay, Nano Covax đã trải qua 3 giai đoạn thử nghiệm lâm sàng, với tổng số gần 14.000 người đã tiêm đủ 2 mũi, trong số này có 12.000 người tham gia giai đoạn 3b đang được theo dõi và lấy mẫu ngày 42 sau tiêm mũi 1, báo cáo chưa trình hội đồng lần này.
Báo cáo đánh giá giữa kỳ giai đoạn 3a trên 1.000 người thử nghiệm, trong đó 60% từ 18-45 tuổi, 22% từ 46-60 tuổi, số còn lại trên 60 tuổi. Trong đó, 3,45% có bệnh lý kèm theo (1 người có tiền sử ung thư, 3 người bệnh tim, 20 người tăng huyết áp, 60 người đái tháo đường...).
Kết quả cho thấy trung bình nồng độ kháng thể Anti-S-IgG đạt 57,56 U/ml, tăng gấp 218.93 lần so với D0 (trước khi tiêm), tỉ lệ chuyển đảo huyết thanh đạt 99,2%. Nhóm nghiên cứu đánh giá vaccine đạt yêu cầu về tính sinh miễn dịch.
Về độ an toàn, sau tiêm vaccine có 38,7% người thử nghiệm cho biết có đau nhẹ, 12% "đau trung bình", 1 người đau nhiều tại vị trí tiêm, 2,6% có đỏ nhẹ tại vết tiêm, 5,4% có ngứa, 2,2% có sưng thành cục cứng tại vị trí tiêm, 2% có buồn nôn, 6,7% có đau cơ... Có 2 người gặp phản ứng phản vệ độ 2 và hồi phục trong ngày tiêm. Số còn lại bình thường.
Nhóm nghiên cứu đánh giá vaccine đạt yêu cầu về sinh miễn dịch và độ an toàn. Hội đồng Đạo đức cũng đã thông qua kết luận này.
Ngoài Nano Covax, trong phiên họp ngày 29-8 sẽ xem xét hồ sơ 1 vaccine nhập ngoại, là vaccine sản xuất tại UAE (công nghệ mua của Hãng Sinopharm).