Cụ thể, với vaccine Covid-19 Nano Covax, sau khi nhà sản xuất và nhóm nghiên cứu nộp hồ sơ hoàn thiện, bổ sung về thử nghiệm lâm sàng và đăng ký vaccine, dự kiến ngày mai (15-9), Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia sẽ họp thẩm định kết quả. Sau đó, Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc sẽ xem xét hồ sơ.
Với vaccine Covivac, ngày 15-9, nhóm nghiên cứu sẽ tiêm thử nghiệm mũi 2 giai đoạn 2 tại tỉnh Thái Bình.
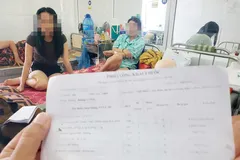
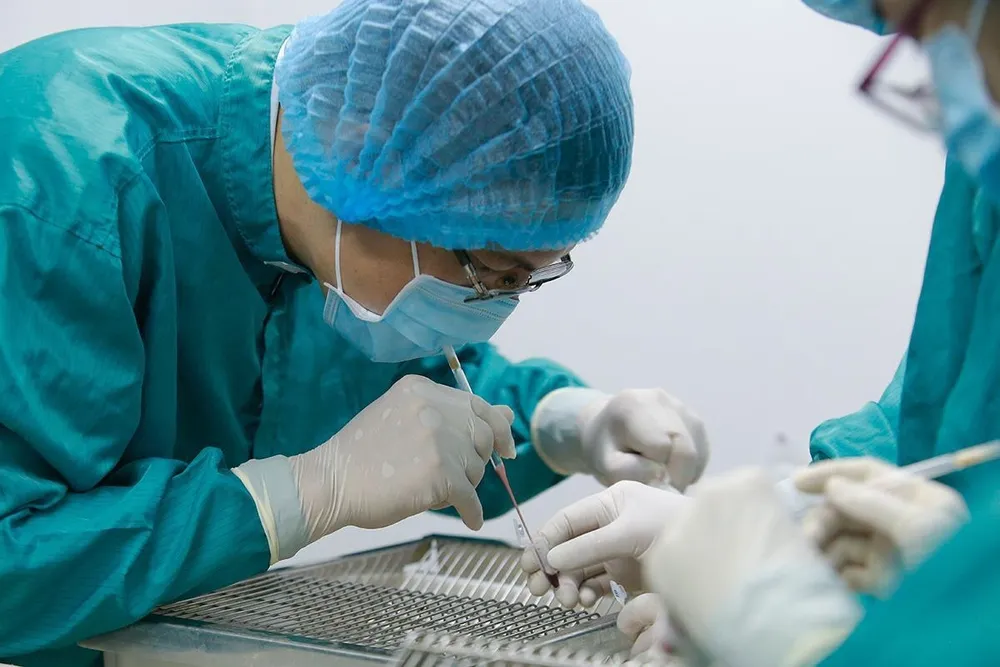 Nano Covax là vaccine Covid-19 đầu tiên của Việt Nam thử nghiệm lâm sàng giai đoạn thứ 3. Đã có gần 14.000 người được tiêm sau hơn 8 tháng tiến hành 3 giai đoạn thử nghiệm lâm sàng.
Nano Covax là vaccine Covid-19 đầu tiên của Việt Nam thử nghiệm lâm sàng giai đoạn thứ 3. Đã có gần 14.000 người được tiêm sau hơn 8 tháng tiến hành 3 giai đoạn thử nghiệm lâm sàng. Cũng theo Bộ Y tế, hiện một số DN của Việt Nam cũng đang trong quá trình đàm phán, ký kết thoả thuận để thử nghiệm lâm sàng và nhận chuyển giao công nghệ sản xuất một số loại vaccine từ nước ngoài.
Tại cuộc họp, các chuyên gia, nhà khoa học nhận định những dự án sản xuất vaccine tại Việt Nam rất khả quan, đến năm 2022 sẽ đi vào hoạt động. Do vậy, cần tính toán lại chiến lược mua, nhập khẩu và thậm chí tiến tới xuất khẩu vaccine.
Với vaccine Covid-19 cho trẻ em, PGS.TS Lê Văn Truyền, Chủ tịch Hội đồng Tư vấn cấp giấy đăng ký thuốc, nguyên liệu làm thuốc, cho biết hiện nay vaccine phòng Covid-19 đa phần để dành cho người lớn và một số hãng mới bắt đầu nghiên cứu để sản xuất vaccine cho trẻ em. Tuy nhiên, các nhà khoa học cho biết về nguyên tắc, các loại vaccine phòng Covid-19 có cơ chế hoạt động, tác động đối với người lớn, trẻ em giống nhau.
Về thuốc điều trị, theo Bộ Y tế, đang có rất nhiều loại thuốc, đặc biệt là loại thuốc kháng virus Molnupiravir hiện trong quá trình thử nghiệm cho thấy hiệu quả điều trị rất tốt. Các nhà khoa học, chuyên gia, Bộ Y tế kỳ vọng sau khi hoàn thành thử nghiệm đánh giá lâm sàng, các DN dược của Việt Nam sẽ làm việc, để có bản quyền sản xuất trong nước. Từ đó tự chủ được nguồn thuốc điều trị sớm cho các bệnh nhân Covid-19.
Về xét nghiệm, theo Bộ Y tế, Việt Nam đã nghiên cứu, phát triển, sản xuất được các loại kit xét nghiệm nhanh kháng nguyên có độ nhạy cao trong phát hiện những biến thể mới của virus SARS-CoV-2. Tuy nhiên, năng lực sản xuất của các doanh nghiệp trong nước còn thấp, nên vẫn nhập khẩu. Một số DN hiện đã tiếp nhận, chuyển giao công nghệ sản xuất kit xét nghiệm nhanh kháng nguyên, chuẩn bị sản xuất.
Thông tin ban đầu cho thấy sinh phẩm xét nghiệm nhanh kháng nguyên được sản xuất trong nước sắp tới sẽ rẻ rất nhiều so với giá thành nhập khẩu hiện nay. Nếu áp dụng xét nghiệm nhanh mẫu gộp thì chi phí xét nghiệm có thể giảm tới hàng chục lần. Nếu Việt Nam tự chủ được nguồn kit xét nghiệm nhanh kháng nguyên thì có thể bán để người dân tự xét nghiệm.
Nano Covax là vaccine Covid-19 đầu tiên của Việt Nam đang thử nghiệm lâm sàng giai đoạn thứ 3. Đã có gần 14.000 người được tiêm thử nghiệm vaccine Nano Covax sau hơn 8 tháng tiến hành 3 giai đoạn thử nghiệm lâm sàng .
Ngày 7-8, Hội đồng đạo đức đã họp khẩn cấp để nghiệm thu kết quả thử nghiệm giai đoạn 1, đánh giá kết quả giữa kỳ thử nghiệm giai đoạn 2 vaccine Nano Covax. Ngày 25-8, Hội đồng đạo đức thông qua báo cáo giữa kỳ giai đoạn 3a, sử dụng các kết quả nghiên cứu thử nghiệm lâm sàng, gửi cho Thường trực Hội đồng tư vấn cấp phép thuốc và nguyên liệu làm thuốc, để xem xét cấp phép khẩn cấp.
Ngày 29-8, Hội đồng tư vấn đề nghị Nanogen tiếp tục bổ sung hồ sơ vaccine Covid-19 Nanocovax. Theo đó, DN cần bổ sung hồ sơ chất lượng; hồ sơ dược lý, lâm sàng, bổ sung tính an toàn của toàn bộ người đã được tiêm ít nhất một liều vaccine, và giải thích rõ về các trường hợp gặp phản ứng nghiêm trọng.
Ngoài ra, hồ sơ cũng cần bổ sung về tính sinh miễn dịch, cập nhật dữ liệu đánh giá tính sinh miễn dịch trên các biến chủng mới, ví dụ chủng Delta, Alpha..